טיפול נוירוכירורגי ברעד ראשוני – רעד ראשוני (Essential Tremor) הוא הפרעת תנועה שכיחה הפוגעת בכ-1% מהאוכלוסיה. ההגדרה ״ראשוני״ מצביעה על כך שאין סיבה ידועה לרעד וכי הרעד הוא הסימפטום היחיד או העיקרי (Haubenberger 2018). אנשים הסובלים מרעד ראשוני מדווחים על פגיעה בתפקוד יומיומי ובאיכות החיים ועל מבוכה חברתית מלווה בשכיחות גבוהה של דיכאון וחרדה.
מטרת הטיפול היא הורדת הרעד על מנת להביא לשיפור בתפקוד ובתפקוד היומיומי. הקו הטיפולי הראשון הוא תרופתי באמצעות תרופות ממשפחת חסמי הבטא. התרופה המקובלת ביותר היא דרלין, ופרזולין (primidone) תרופה נוגדת פרכוסים. תרופות אחרות לא נמצאו כיעילות בשיפור הרעד על ידי האקדמיה האמריקאית לנוירולוגיה (Zesiewicz 2011). לכן מקובל על פי הספרות להציע למטופלים שלא חווים שיפור מספק ברעד לאחר נסיון טיפולי בשתי תרופות אלו, טיפול פולשני נוירוכירורגי. זהו טיפול המתערב במעגלים העצביים במוח שמעורבים ביצירת הרעד.
המטרה המקובלת ביותר להתערבות היא גרעין ה-VIM בתלמוס. הוא מהווה תחנת ממסר למסלולים העצביים בין הצרבלום לקורטקס המוטורי.
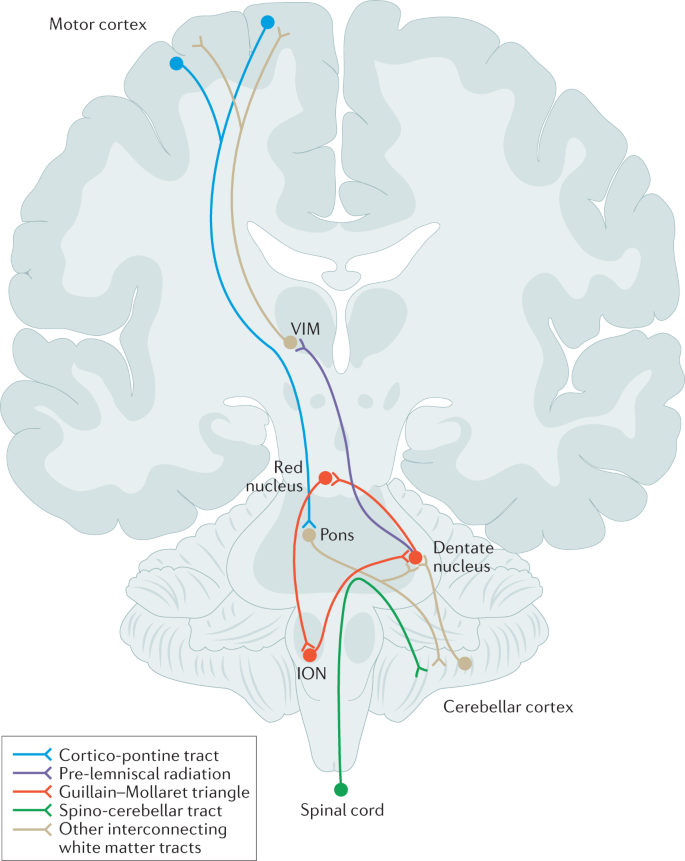
קיימות 3 אפשרויות מקובלות להתערבות נוירכירורגית:
- ניתוח סטריאוטקטי להרס גרעין ה-Vim באמצעות צריבה בגלי רדיו RF (Radiofrequency). ניתוח זה כרוך בפתיחה קטנה של הגולגולת. לאחר מכן, אנו מחדירים אלקטרודה לגרעין ה-Vim שמשמשת לחימום מקומי והרס ממוקד.
- ניתוח סטריאוטקטי להשתלת קוצב מוחי עמוק (DBS – Deep Brain Stimulation). ניתוח זה כרוך בפתיחה קטנה של הגולגולת. זאת על מנת להשתיל אלקטרודה לגרעין ה-Vim שלאחר חיבורה לבטריית קוצב. היא משמשת למתן זרמים חשמליים עדינים. זרמים אלה מווסתים את הפעילות בגרעין ה-Vim ובמסלולים העוברים דרכו.
- צריבה באמצעות אנרגיית אולטרה-סאונד ממוקדת תחת בקרת MRI) MRgFUS – MR guided Focused Ultrasound). בטכניקה זו ממקדים אנרגיה של גלי קול בנקודה מדוייקת בעומק המוח תחת בקרת הטמפרטורה במוח. באמצעות הדמיית MRI בזמן אמת, ועל ידי כך גורמים לחימום מבוקר והרס ממוקד של גרעין ה-Vim (בדומה לצריבה עם RF אך ללא צורך בפתיחת הגולגולת).
טיפול נוירוכירורגי ברעד ראשוני
התערבויות אלו הינן זעיר פולשניות. אך עדיין כמו כל ניתוח מוח כרוכות בסיכון נמוך לנזק נוירולוגי שעלול להיות משמעותי (כגון חולשת צד, הפרעת שוו״מ, הפרעת תחושה). בנוסף, שתי האפשרויות הראשונות כרוכות בניתוח מוח הכולל חתך בעור ופתיחה של הגולגולת. דבר המוסיף סיכון לזיהום ודימום מוחי.
האפשרות השלישית, הטיפול באמצעות MRgFUS. הוא אושר בשנת 2016 על ידי ה-FDA (1) כטיפול ברעד ראשוני לאחר שהוכח כיעיל ובטוח במספר עבודות כולל מחקר פרוסקטיבי רנדומלי (Elias 2017). היתרון של MRgFUS הוא שהצריבה מתבצעת בצורה ״לא פולשנית״. כך אין צורך בפתיחה של הגולגולת, ולכן כרוכה בסיכונים נמוכים יחסית לטיפולים האחרים .
בכל אחת מהשיטות האתגר הניתוחי הוא באיתור המדוייק של גרעין ה-Vim בתלמוס שלא ניתן לזיהוי ב-MRI קליני. קואורדינטות המטרה נקבעות לכן בתחילת הפעולה יחסית לנקודות ייחוס. הן ניתנות לזיהוי במוח (AC – Anterior Commissure; PC – Posterior Commissure ) ולאחר מכן מבוצע זיהוי ותיקון של המטרה הסופית במהלך הניתוח.
בגישות הניתוחיות הפתוחות משתמשים ברישום אלקטרופיזיולוגי של פעילות תאי העצב בעומק המוח. כמו כן בזיהוי דפוס פעילות האופייני לגרעין ה-Vim. רישום זה מתבצע על ידי החדרה של אלקטרודה מיוחדת. הוא מצריך לעיתים ביצוע של מספר ״מסלולים״, דהיינו כניסות למוח עם האלקטרודה עד לזיהוי הגרעין. כל מסלול כרוך כמובן בסיכון קטן נוסף לדמם מוחי ונזק נוירולוגי. לאחר מכן אנו מבצעים גירוי חשמלי. זאת על מנת לוודא את ההשפעה על הרעד בזמן אמת במהלך הניתוח. טרם הצריבה או ההשתלה של האלקטרודה.
יתרונות הטיפול הנוירוכירורגי ברעד ראשוני
היתרון ב- MRgFUS הוא היכולת להדגים בזמן אמת את שינויי הטמפרטורה באזור הצריבה בעומק המוח. יתרון נוסף הוא לבצע לזיה זמנית-הפיכה המפריעה לפעילות העצבית בתלמוס. זאת באמצעות חימום לטמפרטורה נמוכה ובדיקת ההשפעה טרם ביצוע הצריבה הסופית. הטכניקה המקובלת לכן לביצוע הצריבה ב- MRgFUS היא להתחיל בקואורדינטות הממוצעות המקובלות בספרות יחסית ל- AC-PC (11 ממ הצידה מדופן החדר השלישי, כ-25% מהמרחק בין ה-AC-PC קדמית ל-PC). לפי ניתוח קליני של השפעת הלזיה ההפיכה להזיז את אזור החימום. כאשר מזוהה האזור עם ההשפעה המיטבית מבוצעת צריבה בטמפרטורה גבוהה.
המגבלות לביצוע פעולת ה- MRgFUS כרוכות לכן ביכולת להעביר אנרגיית אולטרה-סאונד דרך עצמות הגולגולת. לכן מקובל למדוד טרם ביצוע הפעולה את ה-SDR (Skull Density Ratio).
מבחינת סיבוכים MRgFUS הינה פעולת צריבה (הרס) של אזור בעומק המוח. לכן, למרות שאינה כרוכה בסיכונים של פתיחת הגולגולת עדיין טומנת בחובה סיכונים אפשריים. כמו של נזק נוירולוגי עקב פגיעה במבנים סמוכים. המבנים הסמוכים לגרעין ה-VIM הם הגרעין התחושתי הנמצא אחורית לו, והמסילות העצביות העוברות בקפסולה הפנימית העוברות לטרלית (צידית) ומתחתיו. מסילות אלו אחראיות על התפקודים המוטורים והתחושתיים של הצד הנגדי של הגוף.
