מחלת פרקינסון היא מחלה ניוונית של מערכת העצבים המרכזית (נוירודגנרטיבית) הפוגעת בוויסות התנועה בגוף. הסיבה למחלת הפרקינסון אינה ידועה ברוב המקרים, אם כי זוהו מספר גנים המעורבים במנגנון המחלה. המחלה מופיעה לרוב בגילאי 50-60 ומאופיינת במהלך המתקדם בצורה איטית לאורך שנים. השכיחות המוערכת של מחלת הפרקינסון הוא כ-1-2% מהאוכלוסיה מעל גיל 65.
הסימפטומים העיקריים של המחלה הם מוטוריים וכוללים האטה בתנועות (ברדיקינזיה), נוקשות של תנועת השרירים (ריגידיות), רעד אופייני במנוחה, חוסר קואורדינציה והפרעות בשיווי משקל. בד"כ הסימפטומים מתפתחים תחילה בצד אחד של הגוף. למרות שהרעד הוא המאפיין העיקרי שאנשים מקשרים עם פרקינסון, דווקא הנוקשות והאיטיות הם לרוב הסימפטומים המקשים ביותר על איכות חייהם של החולים במחלה.
בנוסף לסימפטומים המוטוריים ישנם גם סימפטומים לא מוטוריים הכוללים הפרעות שינה, פגיעה בחוש הריח, עצירות, לחץ דם נמוך וירידה קוגניטיבית הדרגתית עד כדי דמנציה בשלבים מתקדמים של המחלה.
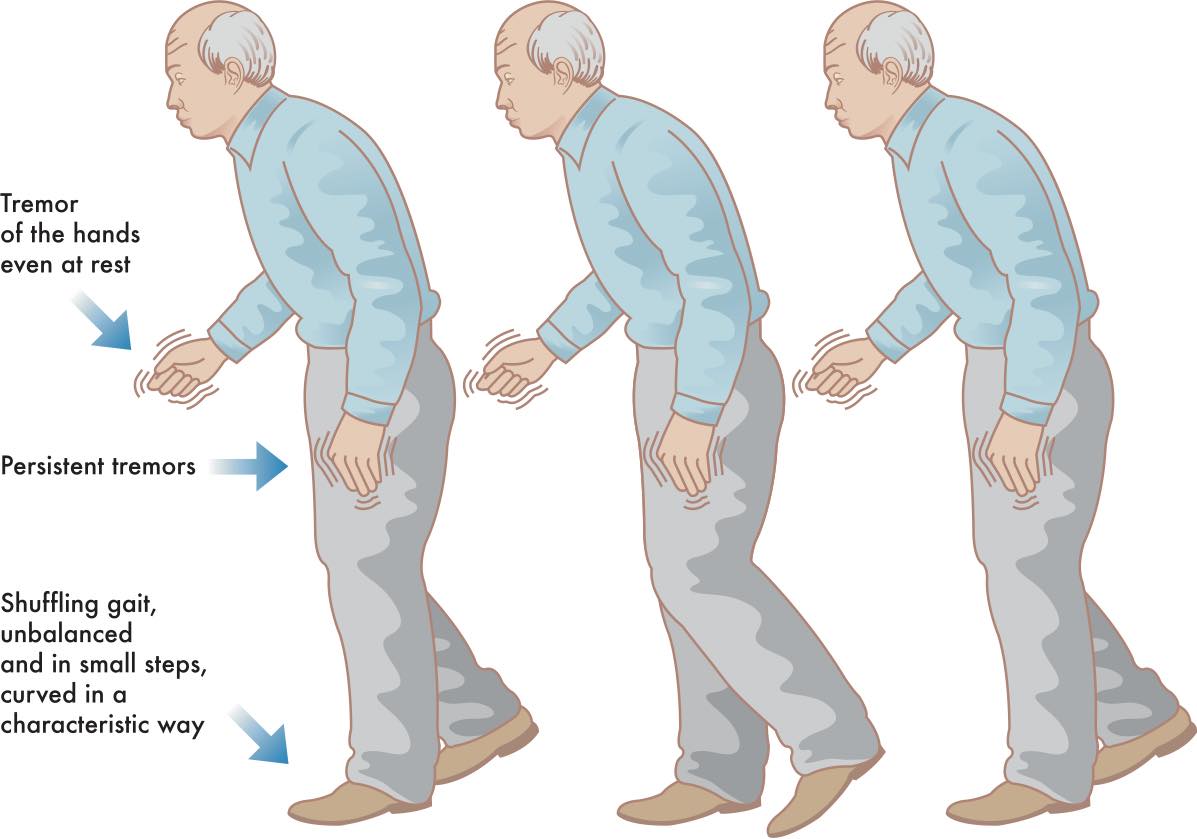
המחלה נגרמת כתוצאה מחוסר במעביר העצבי (נוירוטרנסמיטר) דופמין בגרעיני המוח העמוקים באזור הנקרא הגרעינים הבזאליים (Basal Ganglia). גרעינים אלו במוח אחראיים על תכנון התנועה ובקרתה. באופן תקין מווסת הדופמין את פעילות הגרעינים הבזאליים לכיוון של יצירת תנועה. חוסר של דופמין מקשה לכן על תחילת תנועה ובקרתה ולכן נוצרת האיטיות והרעד האופייניים.
הפתולוגיה במחלת הפרקינסון נגרמת כתוצאה מהתנוונות ומוות הדרגתי של תאים באחד מגרעיני המוח העמוקים באזור הנקרא substantia nigra (החומר השחור). תאים אלו אחראים על ייצור והפרשת הדופמין אל הגרעינים הבזליים וכאשר מספרם יורד גם רמת ההפרשה של דופמין יורדת בהתאמה ומובילה להתפתחות הסימפטומים האופייניים.
הטיפול התרופתי במחלת הפרקינסון
מטרת הטיפול בפרקינסון הוא להקל בסימפטומים ולשפר את איכות חייהם של המטופלים. אין כיום תרופה המרפאת את המחלה. הטיפול מתבסס על העלאת רמות הדופמין במוח או חיקוי של פעולתו במגוון דרכים. התרופה הבסיסית הינה levo-dopa והיא משמשת כחומר מוצא לייצור דופמין וגורמת לעלייה ברמתו במוח. תרופה זו יעילה ביותר בשלבים הראשונים של המחלה אולם יעילותה פוחתת עם משך הטיפול ונזקקים לכמויות הולכות ועולות עד שלאחר תקופה מסויימת מופיעות תופעות לוואי הכוללות חוסר יציבות מבחינת הסימפטומים המוטוריים (פלוקטואציות מוטוריות) המתבטאות כתקופות בהן המטופל סובל מתנועות יתר לא רצוניות (דיסקינזיות) ותקופות בהן הוא קופא (Freezing) העלול להוביל לנפילות ופציעות חמורות (On-Off periods).
הטיפול הניתוחי במחלת הפרקינסון
גרייה מוחית עמוקה (Deep Brain Stimulation- DBS)
בחולים במחלת הפרקינסון בהם הטיפול התרופתי אינו יעיל עוד יכול טיפול ניתוחי על ידי השתלת קוצב מוחי ואלקטרודות לגרייה מוחית עמוקה (Deep Brain Stimulation – DBS) בגרעינים הבאזליים להביא לשיפור משמעותי בתסמיני המחלה העיקריים, בעיקר ברעד ובנוקשות האופיניים למחלה. הטיפול מבוסס על היכולת לווסת פעילות של רשתות עצביות במוח באמצעות גירוי חשמלי. שיטה זו התפתחה בשנים האחרונות כגישה טיפולית חדשה ומבטיחה עם למעלה מ-100,000 שתלים ברחבי העולם. השתלת אלקטרודות גירוי מוח עמוק היא פרוצדורה מאושרת ע"י ה-FDA לטיפול במחלת פרקינסון, רעד, דיסטוניה, והפרעה טורדנית כפייתית. חולים שעברו ניתוח בשל התוויות אלו השיגו שיפור משמעותי בתפקוד כללי, עצמאות, איכות חיים, חזרה לעבודה, יכולת לבצע פעולות יומיומיות וזאת בנוסף לשיפור בתסמיני מחלתם הבסיסית כמו רעד, טונוס מוגבר, נוקשות ואיטיות תנועה.
המועמדים לטיפול ניתוחי זה הינם, כאמור, חולי פרקינסון או רעד מסוגים שונים, שעברו הערכה קדם ניתוחית ביחידה להפרעות תנועה, הכוללת בדיקה קלינית של נוירולוג המתמחה בהפרעות תנועה,, MRI ו-CT ונמצאו מתאימים לטיפול זה. הטיפול מבוצע על ידי נוירוכירורג (מנתח מוח) בעל תת-התמחות מיוחדת בתחום. הניתוח מבוצע לרוב בהרדמה מקומית של החולה, על-מנת להשיג את שיתוף הפעולה שלו בזמן הניתוח לשם מיקום אופטימאלי של האלקטרודה. יש לציין כי החולה לא מרגיש כל כאב בזמן הניתוח מכיוון שבאזורים אלה בתוך המוח אין עצבי כאב.
שיטה זו משיגה שליטה ברעד או בסימפטומים אחרים של המחלה, ללא הרס של תאים או פגיעה ברקמת המוח. כמו כן, הגירוי הינו פעולה עדינה ומווסתת שבמידה ולא מושגת בה התוצאה הרצויה, ניתן תמיד להפסיק אותה ו/או לשנות את עוצמת הגירוי בהתאם לצורך.
מהלך הניתוח
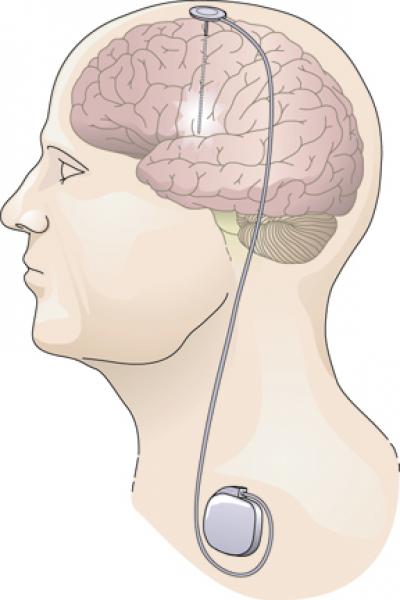
המערכת מורכבת משני חלקים עקריים (ראה תמונה מעלה): אלקטרודות המוחיות ובטריית הקוצב המושתלת בדומה לקוצב לב בדופן בית החזה. הפרוצדורה היא פרוצדורה סטריאוטקטית, דהיינו מאפשרת להגיע לנקודה מדוייקת בעומק המוח. לצורך כך עוברים המטופלים הדמייה מוחית ברזולוציה גבוהה המדגימה הן את גרעיני המוח העמוקים והן את כלי הדם המוחיים ומאפשרת לבצע את הניתוח בדיוק מירבי ובביטחון מקסימלי. הניתוח מבוצע בשני חלקים:
בחלק הראשון מושתלות האלקטרודות המוחיות והוא מבוצע בד"כ בעירות על מנת לאפשר ווידוא של המיקום המיטבי של האלקטרודות להשגת האפקט הקליני הרצוי, תוך מזעור תופעות הלוואי.
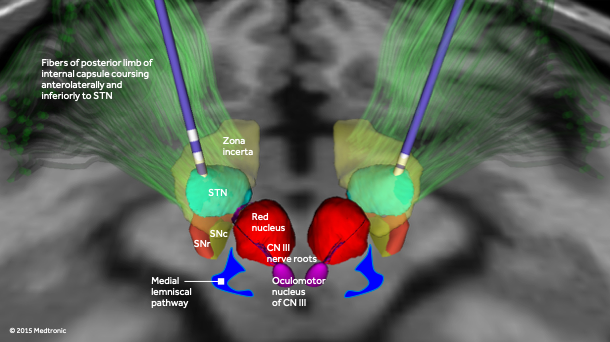
ברגע שהושתלו האלקטרודות עוברים לחלק השני של השתלת הקוצב בדופן בית החזה, במהלך חלק זה אין צורך בניטור המטופל והוא מבוצע בד"כ תחת הרדמה כללית.
תופעות הלוואי של הטיפול הן בדרך כלל משניות לגירוי חשמלי של אזורים סמוכים במוח כאשר מיקום האלקטרודות איננו אופטימלי ולכן החשיבות לבצע את ההליך במרכז המתמחה בניתוחים מסוג זה. הסיבוכים האפשריים בטיפול קשורים לכשל של המערכת המושתלת ובעיקר לנתק במערכת או לזיהומים העלולים להופיע באחוז קטן מהמטופלים. במידה ומתפתח זיהום יש לעיתים צורך להוציא את המערכת המושתלת. הסיכון לדמם מוחי בטכניקות הניתוחיות החדשות בעזרת רובוט הינו נמוך מ-1% .
